El Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) autorizó el protocolo de investigación del ensayo “Solidaridad” de vacunas, patrocinado por la Organización Mundial de la Salud (OMS).
El Grupo de Investigación Clínica de la Dirección de Medicamentos y Productos Biológicos y la Sala Especializada de Dispositivos Médicos y Reactivos de Diagnóstico In Vitro del Instituto evaluaron de manera conjunta la información allegada para que Colombia pudiera sumarse al ensayo, que pretende reunir información sobre la eficacia y seguridad de distintas vacunas contra la covid-19, a través del diseño de un estudio “altamente innovador”.
Inicialmente, Colombia participará con dos tipos de vacunas: la MVC-COV190115 desarrollada por la compañía Medigen Vaccine Biologics Corp, una vacuna de virus vivo atenuado, y la INO-4800, desarrollada por Inovio Pharmaceuticals, que utiliza una tecnología de ácido desoxirribonucleico (ADN) y vincula además el uso de un dispositivo de electroporación llamado CELLECTRA™ 200.
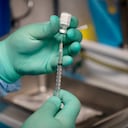
El ensayo internacional a gran escala, aleatorizado y controlado está diseñado con el objetivo de lograr una evaluación rápida, eficiente y confiable de las vacunas candidatas en fase de desarrollo contra el SARS-CoV-2, en lo que tiene que ver con su seguridad y eficacia, e identificar aquellas que serán apropiadas para retrasar la progresión del coronavirus.
Colombia fue elegida entre 20 países candidatos a nivel mundial y como uno de los seis países de la Región de las Américas en participar en este ensayo clínico, entre los que se encuentran Argentina, Brasil, Chile, El Salvador y México.
El estudio “Solidaridad” cuenta con un diseño adaptativo. Es decir, se espera que ingresen otros tipos de vacunas durante el desarrollo, con la participación de 120.000 voluntarios a nivel mundial y alrededor de 40.000 en Colombia. La duración será de cerca de 15 meses.
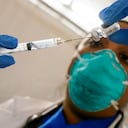
Los participantes en Colombia serán voluntarios de 16 años o más que residan en lugares con alta incidencia del virus al SARS-CoV-2, o que vivan o tengan circunstancias que representen un riesgo importante de exposición como, por ejemplo, el talento humano en salud, especialmente los trabajadores de primera línea, empleados en áreas esenciales en áreas que siguen sin tener acceso a vacunas.
El ensayo clínico fue autorizado, inicialmente, para desarrollarse en la clínica Colsanitas S. A. Sede Clínica Universitaria ubicada en la ciudad de Bogotá, teniendo como investigador principal de este ensayo al doctor Julio Alberto Chacón Sarmiento. No obstante, en el estudio clínico podrán participar las instituciones certificadas en Buenas Prácticas Clínicas (BPC) o aquellas que cuenten con el aval de una entidad certificada de acuerdo con lo dispuesto por la Resolución 730 de 2020.

“El desarrollo en el país de estos ensayos clínicos es un reconocimiento a la rigurosidad sanitaria de Invima y permite llevar a cabo procesos que aporten información a la evaluación de los biológicos y datos clínicos necesarios para determinar la viabilidad de posibles alternativas profilácticas y terapéuticas para el tratamiento de enfermedades como covid-19 en el marco de los lineamientos internacionales de Buenas Prácticas Clínicas, así como el acceso de la población colombiana a este tipo de iniciativas”, resaltó el Invima en el comunicado.