El control de la venta de sustancias moldeantes estará regulada por el Ministerio de Salud, de acuerdo con lo establecido en el artículo 6 de la Ley 2316 de 2023.
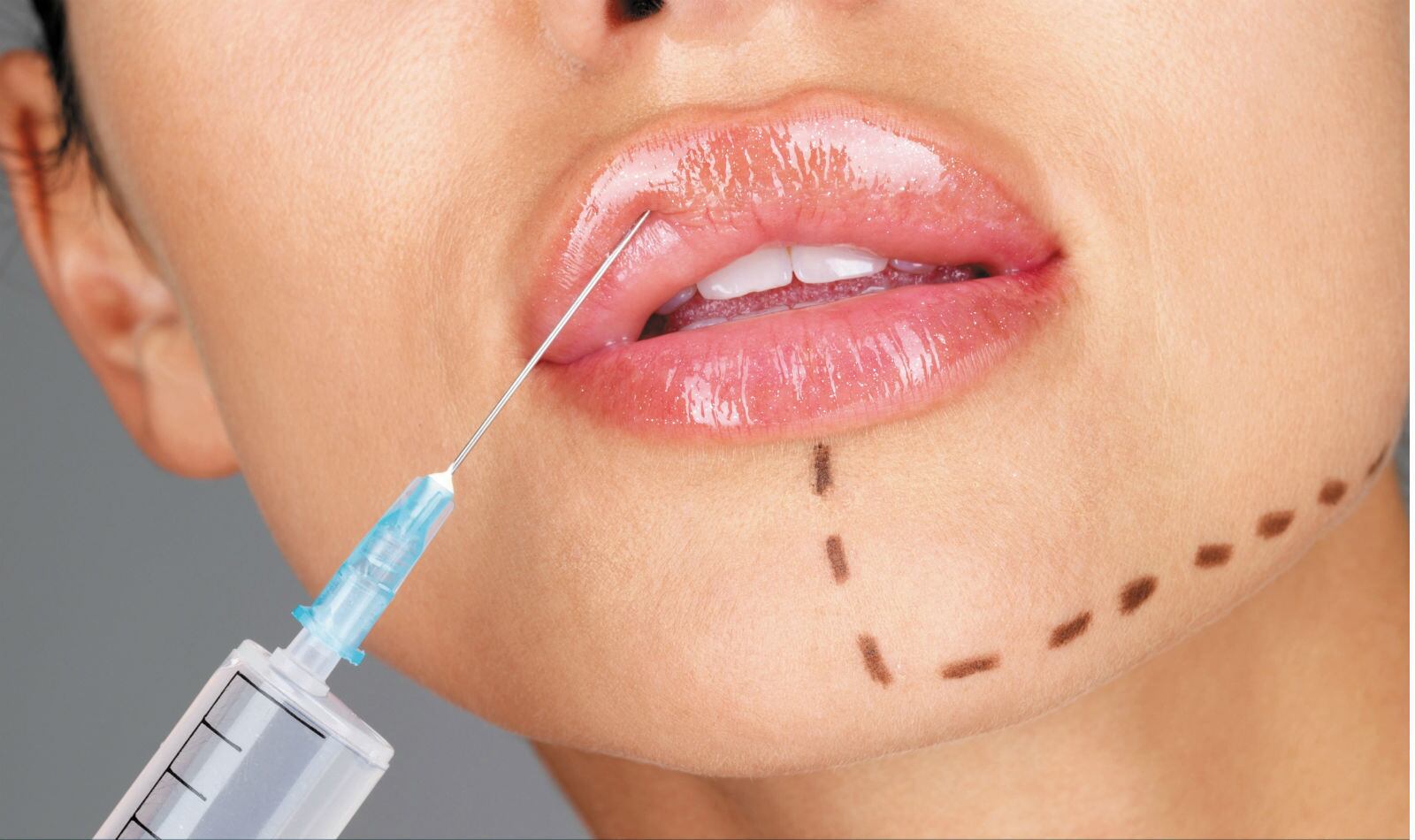

¿Qué incluye el documento regulatorio?
El documento define las transacciones primarias, secundarias y finales de sustancias modelantes permitidas, al establecer la obligación de reportar todo tipo de datos sobre estas, en un sistema de información administrado por el Ministerio de Salud y el Invima.
Además, en el mismo documento se especifica que los datos que deben reportarse para cada tipo de transacción y los plazos para hacerlo, asignando unas funciones de inspección, vigilancia y control sobre este registro a la Superintendencia Nacional de Salud, secretarías de salud e Invima.
Bajo este punto de vista, en el decreto se le ordena al Ministerio poner a disposición todos los documentos necesarios para que se pueda hacer de forma correcta la operación de registro dentro de los 3 meses siguientes a la entrada en vigencia del decreto.
El objetivo de esta norma es el de generar trazabilidad sobre el comercio y aplicación de las sustancias modelantes permitidas, a través del reporte obligatorio de información por parte de los actores involucrados, protegiendo de esta forma la salud de los colombianos que buscan tener acceso a estos elementos.
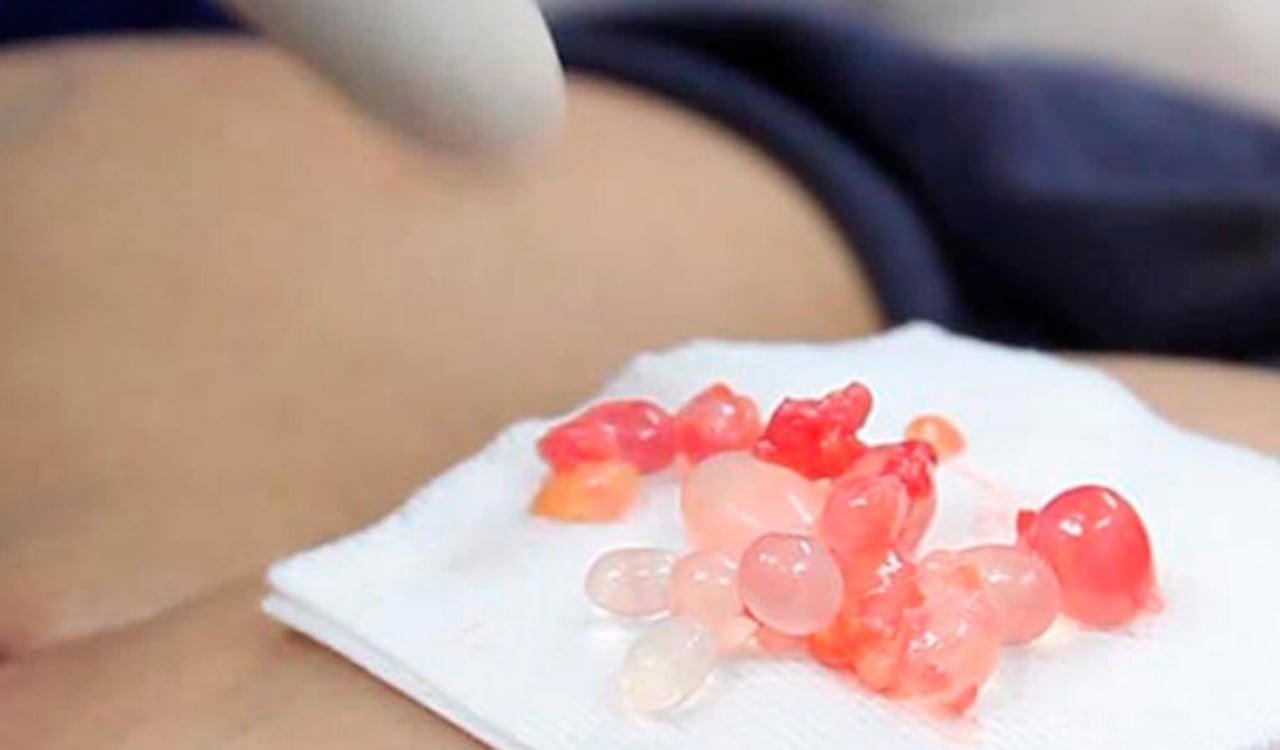

¿Cuáles son las transacciones que deben reportarse?
En el listado expedido por el Ministerio de Salud en colaboración con el Invima, se establecen tres tipos de transacciones que deben reportarse:
- Primarias: primera venta/compra en Colombia
- Secundarias: ventas por actores distintos al fabricante/importador
- Finales: suministro o inyección al usuario final

El documento firmado por el Ministro de Salud, Guillermo Alfonso Jaramillo, especificó los datos que deben reportarse para cada transacción, entre los que se pueden nombrar: identidad de los actores, registro sanitario, lote, cantidad, sitio anatómico de aplicación, entre otros.
De igual forma, se fijaron plazos precisos para el reporte de la información, los cuales estarán entre el 25 del mismo mes y el 10 del siguiente mes, según la fecha de transacción.
Igualmente, se encarga al Ministerio de Salud el diseño y puesta en marcha del sistema informático para el registro, con apoyo del Invima, de acuerdo a las leyes de protección de datos personales.
Es importante mencionar que quien efectúe una transacción sobre sustancias sujetas a registro, será responsable de la información suministrada en el sistema que creará el Invima, por lo que en cualquier momento, las autoridades sanitarias podrán requerir el suministro inmediato de los soportes de la información que se reporta en el aplicativo.
Finalmente, el nuevo capítulo ordena implementar la operación del registro máximo 3 meses después de entrada en vigencia.